Резонансная структура фенола

1. Впечатления от резонансной структуры фенола
1. Широкое применение фенола
Фенол, «всевозможные» в области органической химии, сияет во многих областях. В области медицины это ключевое сырье для синтеза аспирина и других важных лекарств, сопровождающих здоровье человека; в химической промышленности это «основная сила» в производстве фенольной смолы, помогающая развитию материаловедения; в повседневной жизни, Он также используется в качестве дезинфицирующего сырья для защиты нашего здоровья и безопасности. С таким широким спектром применений фенол стал одной из горячих точек в исследованиях органической химии.
2. привести к концепции резонансной структуры
В удивительном мире органической химии резонансные структуры являются уникальной теоретической моделью. Это как волшебный ключ, который может помочь нам открыть дверь в тайну распределения электронов внутри молекулы. Для фенола резонансная структура является ключом к пониманию его свойств.
3. Предложить цель исследования
В этой статье мы глубоко проанализируем резонансную структуру фенола, исследуем внутреннюю связь между ним и свойствами фенола и предоставим теоретическую основу для лучшего понимания и использования фенола.
2. Формирование, характеристики и эффекты резонансная структура фенола
1. Механизм формирования резонансной структуры фенола
(1) Основы молекулярной структуры
Фенол состоит из бензольного кольца и гидроксильной группы. Бензольное кольцо имеет уникальную структуру большой связи, в которой электроны могут свободно перемещаться по кольцу. Атомы кислорода, с другой стороны, имеют одинокую пару электронов, которые, как «эльфы», спрятаны в темноте, ожидая чудесной реакции с бензольным кольцом.
(2) Процесс делокализованный электроном
Когда образуется молекула фенола, одинокая пара электронов атома кислорода сильно взаимодействует с большой связью бензольного кольца. Электроны больше не ограничены конкретным атомом, а перераспределяются внутри молекулы, образуя множественные формулы предела резонанса. Это как замечательный танцевальный спектакль, электронный бесплатный челнок в молекулах, исполняющий уникальный «электронный танец».
(3) Наложение резонансного предельного типа
Эти формулы предела резонанса не существуют независимо, а накладываются друг на друга посредством резонанса. Они похожи на группу «членов команды», работающих вместе, чтобы описать истинное распределение электронного облака молекулы фенола. Именно эта суперпозиция придает молекуле фенола его уникальные свойства.
2. Характеристики структуры резонанса фенола
(1) Высокая плотность соседнего пара-электронного облака
Из-за резонансного эффекта плотность электронного облака соседних и пара положений на бензольном кольце значительно увеличивается. Из принципиальной схемы, электронные облака в этих двух положениях похожи на «зажженные» лампочки, которые особенно привлекательны. Эта высокая плотность электронного облака делает орто-и пара-сайты более активными в химических реакциях.
(2) делокализация отрицательного заряда
Отрицательный заряд на бензольном кольце произошел делокализованный феномен, подобно группе свободных птиц, свободно летающих в «небе» бензольного кольца. Эта делокалитность снижает молекулярную энергию и делает структуру более стабильной, что закладывает основу для химических свойств фенола.
3. Влияние резонансной структуры на свойства фенола
(1) Реактивность
Реакция электрофильного замещения: высокая плотность орто-пара электронного облака делает фенол более склонным к реакции электрофильного замещения. Например, при нитрации, сульфонирования и других реакциях реагенты будут преимущественно атаковать орто-и пара-положения для получения соответствующих продуктов, и продукты в основном сосредоточены в орто-и пара-положениях.
Реакционная селективность: в некоторых реакциях фенол проявляет специфическую реакционную селективность из-за резонансной структуры. Так же, как придирчивый едок, выбирающий только «еду», он любит, эта избирательность дает больше возможностей для органического синтеза.
(2) Кислотность
Резонансная структура облегчает диссоциацию фенольного гидроксила, тем самым повышая кислотность фенола. По сравнению со спиртами, фенол значительно более кислый, как более «едкая» молекула, с большей вероятностью высвобождает ионы водорода.
(3) Стабильность
Энергия резонансной стабилизации уменьшает энергию молекулы фенола, делая ее структуру более стабильной и менее склонной к разложению или изменению. Это делает фенол более надежным в хранении и использовании, и дает гарантию на его широкое применение.
4. Нарисуйте резонансную структуру фенола.
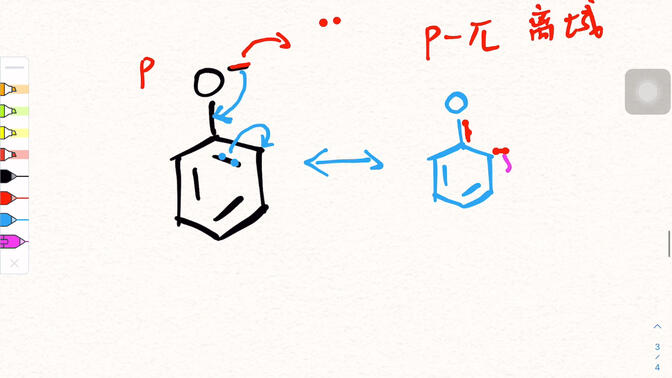
Резонансная структура фенола может быть представлена с помощью простой схематической диаграммы.
Основная структура фенола представляет собой гидроксильную группу (- OH), присоединенную к бензольному кольцу.
Резонансное предельное уравнение-исходная структура фенола, в которой в делокализации не участвуют одинокие электроны атома кислорода;
В другом предельном уравнении одинокая пара электронов атома кислорода взаимодействует с большой & pi; -связью бензольного кольца, образуя частичную двойную связь, характерную для атома кислорода и бензольного кольца. В то же время плотность соседних и пара-электронных облаков на бензольном кольце увеличивается, а направление движения электронов указывается стрелками. Множественные предельные уравнения накладываются для описания истинного распределения электронного облака фенола.
3. Проявление резонансной структуры в реакции фенола
1. Конкретные случаи реагирования
Реакция фенола с бромной водой является классическим случаем. Когда в раствор фенола по каплям добавляют воду брома, сразу же образуется белый осадок, который представляет собой трибромфенол.
2. Совмещенный с анализом структуры резонанса
С точки зрения резонансной структуры, атом брома с большей вероятностью атакует эти две позиции из-за высокой плотности орто-и пара-электронных облаков фенола. Во время реакции атомы брома постепенно заменяют атомы водорода на бензольном кольце, и, наконец, образуется белый осадок трибромфенола. Этот процесс наглядно демонстрирует важную роль резонансной структуры в объяснении химической реакции фенола.
3. Подчеркните роль резонансных структур
Благодаря этому случаю у нас есть более глубокое понимание резонансной структуры-это не только теоретическое понятие, но и ключ к пониманию природы химической реакции фенола. Это как бесшумный проводник, направляющий химическую реакцию.
4. Значение и перспектива изучения резонансной структуры фенола
Резонансная структура делает фенол уникальным реакционной активностью, кислотностью и стабильностью, что дополнительно определяет применение фенола в различных областях. В будущем мы можем объединить передовые методы вычислительной химии и экспериментальные методы для дальнейшего изучения резонансной структуры фенола. Это поможет нам понять природу и поведение фенола более всесторонне, обеспечит более теоретическую поддержку и практическое руководство для развития органической химии и позволит «универсалу» фенола играть большую роль в большем количестве областей.

