Estrutura de ressonância do fenol

1. Impressões da estrutura da ressonância do fenol
1. A aplicação larga do fenol
O fenol, o "todo-agitado" no campo da química orgânica, brilha em muitos campos. No campo da medicina, é a principal matéria-prima para a síntese de aspirina e outras drogas importantes, acompanhando a saúde humana; na indústria química, é a "força principal" na produção de resina fenólica, ajudando o desenvolvimento da ciência dos materiais; na vida diária, Também é usado como matérias-primas desinfetantes proteger nossa saúde e segurança. Com uma gama tão ampla de aplicações, o fenol tornou-se um dos pontos quentes na pesquisa de química orgânica.
2. Levar ao conceito de estrutura de ressonância
No maravilhoso mundo da química orgânica, as estruturas ressonantes são um modelo teórico único. É como uma chave mágica que pode nos ajudar a abrir a porta para o mistério da distribuição de elétrons dentro da molécula. Para o fenol, a estrutura de ressonância é a chave para entender suas propriedades.
3. Propor o objetivo do estudo
Neste trabalho, analisaremos profundamente a estrutura de ressonância do fenol, exploraremos a relação interna entre ele e as propriedades do fenol, e forneceremos uma base teórica para melhor compreendermos e utilizarmos o fenol.
2. Formação, características, e efeitos da estrutura da ressonância do fenol
1. Mecanismo de formação da estrutura de ressonância do fenol
(1) Base da estrutura molecular
Fenol consiste em um anel benzênico e um grupo hidroxila. O anel de benzeno tem uma estrutura única de ligação grande na qual os elétrons podem se mover livremente por todo o anel. Os átomos de oxigênio, por outro lado, têm pares soltos de elétrons, que são como "elfos" escondidos no escuro, esperando por uma reação maravilhosa com o anel de benzeno.
(2) O elétron deslocalizou o processo
Quando a molécula de fenol é formada, os elétrons do par solitário do átomo de oxigênio interagem fortemente com a grande ligação & pi; do anel benzênico. Os elétrons não estão mais confinados a um átomo particular, mas são redistribuídos dentro da molécula, formando múltiplas fórmulas limite de ressonância. Isto é como uma performance de dança maravilhosa, transporte eletrônico gratuito nas moléculas, realizando uma "dança eletrônica" única.
(3) Superposição do tipo limite de ressonância
Essas fórmulas limite de ressonância não existem independentemente, mas são sobrepostas umas às outras através da ressonância. Eles são como um grupo de "membros da equipe" trabalhando juntos para descrever a verdadeira distribuição da nuvem eletrônica da molécula de fenol. É essa superposição que dá à molécula fenol suas propriedades únicas.
2. Phenol ressonância estrutura características
(1) alta densidade de adjacente para elétron nuvem
Devido ao efeito de ressonância, a densidade da nuvem de elétrons das posições adjacentes e para no anel benzênico aumenta significativamente. A partir do diagrama esquemático, as nuvens de elétrons nessas duas posições são como lâmpadas "acesas", que são particularmente atraentes. Essa alta densidade de nuvens eletrônicas torna os sítios orto e para mais ativos em reações químicas.
(2) a deslocalização da carga negativa
Carga negativa sobre o anel de benzeno ocorreu fenômeno deslocalizado, como um grupo de aves livres, voando livremente no "céu" do anel de benzeno. Esta deslocalidade reduz a energia molecular e torna a estrutura mais estável, o que estabelece as bases para as propriedades químicas do fenol.
3. Efeito da estrutura de ressonância nas propriedades do fenol
(1) Reatividade
Reação eletrofílica de substituição: A alta densidade da nuvem de elétrons orto-para torna o fenol mais propenso à reação eletrofílica de substituição. Por exemplo, na nitração, sulfonação e outras reações, os reagentes atacarão preferencialmente as posições orto e para para para gerar produtos correspondentes, e os produtos são concentrados principalmente nas posições orto e para.
Seletividade da reação: Em algumas reações, o fenol exibe uma seletividade específica da reação devido à estrutura da ressonância. Assim como um comedor exigente, escolhendo apenas o "alimento" que ele gosta, essa seletividade oferece mais possibilidades para a síntese orgânica.
(2) acidez
A estrutura de ressonância facilita a dissociação do hidrogênio hidroxila fenólico, aumentando assim a acidez do fenol. Comparado com álcoois, o fenol é significativamente mais ácido, como uma molécula mais “pungente”, mais propensa a liberar íons de hidrogênio.
(3) Estabilidade
A energia de estabilização por ressonância reduz a energia da molécula fenol, tornando sua estrutura mais estável e menos propensa à decomposição ou alteração. Isso torna o fenol mais confiável no armazenamento e uso, e fornece uma garantia para sua ampla aplicação.
4. Desenhe a estrutura de ressonância do fenol
A estrutura de ressonância do fenol pode ser apresentada por um diagrama esquemático simples.
A estrutura básica do fenol é um grupo hidroxila (- OH) ligado ao anel benzeno.
Uma equação limite de ressonância é a estrutura original do fenol, na qual os elétrons do par solitário do átomo de oxigênio não participam da deslocalização;
Em outra equação limite, o par solitário elétron do átomo de oxigênio interage com a grande ligação & pi; do anel de benzeno, formando uma característica de ligação dupla parcial entre o átomo de oxigênio e o anel de benzeno. Ao mesmo tempo, a densidade das nuvens de elétrons adjacentes e para no anel de benzeno aumenta e a direção do movimento dos elétrons é indicada por setas. Equações limite múltiplas são sobrepostas para descrever a verdadeira distribuição de nuvens eletrônicas de fenol.
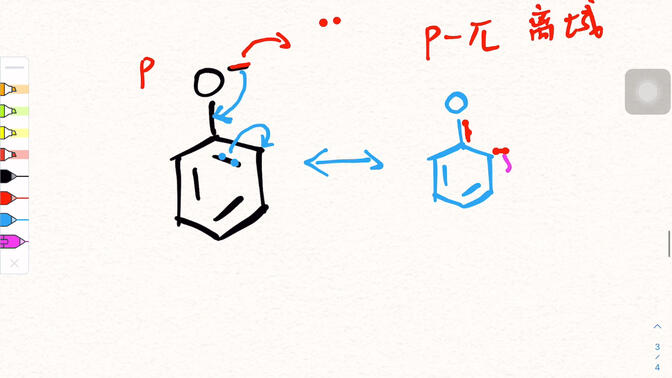
3. A manifestação da estrutura da ressonância na reação do fenol
1. Casos específicos resposta
A reação de fenol com água bromo é um caso clássico. Quando a água de bromo é adicionada gota a gota à solução de fenol, um precipitado branco é imediatamente produzido, que é o tribromofenol.
2. Combinado com a ressonância estrutura análise
Do ponto de vista da estrutura de ressonância, o átomo de bromo é mais propenso a atacar essas duas posições devido à alta densidade das nuvens orto-e para-elétrons do fenol. Durante a reação, os átomos de bromo substituem gradualmente os átomos de hidrogênio no anel benzeno e, finalmente, um precipitado branco de tribromofenol é gerado. Este processo demonstra claramente o importante papel da estrutura de ressonância na explicação da reação química do fenol.
3. Enfatizar o papel das estruturas ressonantes
Através deste caso, temos uma compreensão mais profunda de que a estrutura de ressonância não é apenas um conceito teórico, mas também a chave para entender a natureza da reação química do fenol. É como um condutor silencioso, guiando a reação química.
4. O valor e perspectiva de estudar a estrutura de ressonância do fenol
A estrutura de ressonância faz com que o fenol tenha reatividade, acidez e estabilidade únicas, o que determina ainda mais a aplicação do fenol em diversos campos. No futuro, podemos combinar métodos avançados de química computacional e técnicas experimentais para estudar melhor a estrutura de ressonância do fenol. Isso nos ajudará a entender a natureza e o comportamento do fenol de forma mais abrangente, fornecer mais suporte teórico e orientação prática para o desenvolvimento da química orgânica e deixar o "generalista" do fenol desempenhar um papel maior em mais campos.

