Struktur resonans phenol

1. Jejak struktur resonans Phenol
1. Permohonan luas phenol
Phenol, "all-ronged dalam" dalam bidang kimia organik, bersinar dalam pelbagai bidang. Dalam bidang perubatan, ia adalah bahan mentah utama untuk sintesis aspirin dan lain-lain ubat penting, telekonferensi kesihatan manusia; Dalam industri kimia, ia adalah "daya utama" dalam pengeluaran resin fenolik, membantu pembangunan sains bahan; Dalam kehidupan seharian, Ia juga digunakan sebagai bahan mentah disinfektan menjaga kesihatan dan keselamatan kami. Dengan pelbagai aplikasi sedemikian, phenol telah menjadi salah satu tempat panas dalam penyelidikan kimia organik.
2. Membawa kepada konsep struktur resonans
Dalam dunia kimia organik yang indah, struktur resonan adalah model teoritis yang unik. Ia adalah seperti kunci ajaib yang boleh membantu kita membuka pintu kepada misteri pengedaran elektron di dalam molekul. Untuk phenol, struktur resonans adalah kunci untuk memahami sifatnya.
3. Mencadangkan tujuan kajian
Dalam kertas ini, kami akan menganalisis struktur resonans fenol secara mendalam, meneroka hubungan dalaman di antara ia dan sifat fenol, dan menyediakan asas teori bagi kita untuk memahami dan menggunakan fenol dengan lebih baik.
2. Pembentukan, ciri-ciri dan kesan struktur resonans Phenol
1. Pembentukan mekanisme resonans struktur phenol
(1) asas struktur molekul
Phenol terdiri daripada cincin benzene dan kumpulan hydroxyl. Cincin benzene mempunyai yang unik besar & pi; Struktur bon di mana elektron boleh bergerak secara bebas sepanjang cincin tersebut. Atom oksigen, di sisi lain, mempunyai pasangan tunggal elektron, yang seperti "elves" tersembunyi dalam gelap, menunggu reaksi yang indah dengan cincin benzena.
(2) proses delocalized elektron
Apabila molekul phenol dibentuk, elektron pasangan lone atom oksigen berinteraksi kuat dengan besar & pi; Ikatan cincin benzene. Elektron tidak lagi terhad kepada atom yang tertentu, tetapi akan diulang dalam molekul, membentuk pelbagai resonans had formula. Ini seperti persembahan tarian yang indah, ulang-alik percuma elektronik dalam molekul, melaksanakan "tarian elektronik" yang unik.
(3) Superposition jenis had resonans
Formula had resonans ini tidak wujud secara bebas, tetapi akan melapisi antara satu sama lain melalui resonans. Mereka adalah seperti sekumpulan "team members" bekerja bersama-sama untuk menggambarkan pengagihan awan elektron benar molekul phenol. Ia adalah superposition ini yang memberikan molekul phenol sifatnya yang unik.
2. Ciri-ciri struktur resonans Phenol
(1) ketumpatan tinggi awan elektron perenggan bersebelahan
Oleh kerana kesan resonans, ketumpatan awan elektron kedudukan bersebelahan dan perenggan pada cincin benzena meningkat dengan ketara. Dari gambarajah skematik, awan elektron dalam dua jawatan ini adalah seperti "lit" mentol, yang amat menarik perhatian. Ketumpatan awan elektron tinggi ini menjadikan tapak ortho dan perenggan lebih aktif dalam tindak balas kimia.
(2) delocalization caj negatif
Caj negatif pada cincin benzene berlaku fenomena delocalized, seperti sekumpulan burung percuma, terbang secara bebas dalam "sky dalam" cincin benzene. Delocality ini mengurangkan tenaga molekul dan menjadikan struktur lebih stabil, yang meletakkan asas bagi sifat-sifat kimia phenol.
3. Kesan struktur resonans pada sifat-sifat phenol
(1) kereaktifan
Tindak balas penggantian electrophilic: ketumpatan tinggi awan elektron ortho-perenggan membuat phenol lebih terdedah kepada tindak balas penggantian electrophilic. Sebagai contoh, dalam nitration, sulfonation dan reaksi lain, reactants yang preferentially akan menyerang kedudukan ortho dan perenggan untuk menjana produk yang sepadan, dan produk-produk terutamanya tertumpu dalam kedudukan ortho dan perenggan.
Tindak balas 'selectivity': dalam beberapa reaksi, phenol mempamerkan 'selectivity' tindak balas tertentu disebabkan oleh struktur resonans. Sama seperti pemakan pemilih, memilih hanya "makanan" yang dia suka, selektiviti ini memberikan lebih banyak kemungkinan untuk sintesis organik.
(2) keasidan
Struktur resonans menjadikannya lebih mudah untuk hidrogen hidroksil fenolik untuk memisahkan, dengan itu meningkatkan keasidan fenol. Berbanding dengan alkohol, phenol adalah jauh lebih berasid, seperti "spicy yang lebih banyak" molekul, lebih cenderung untuk melepaskan ion hidrogen.
(3) kestabilan
Tenaga penstabilan resonans mengurangkan tenaga molekul phenol, membuat struktur yang lebih stabil dan kurang terdedah kepada penguraian atau perubahan. Ini menjadikan fenol lebih dipercayai dalam penyimpanan dan penggunaan, dan memberikan jaminan untuk aplikasinya yang luas.
4. Lukis struktur resonans phenol
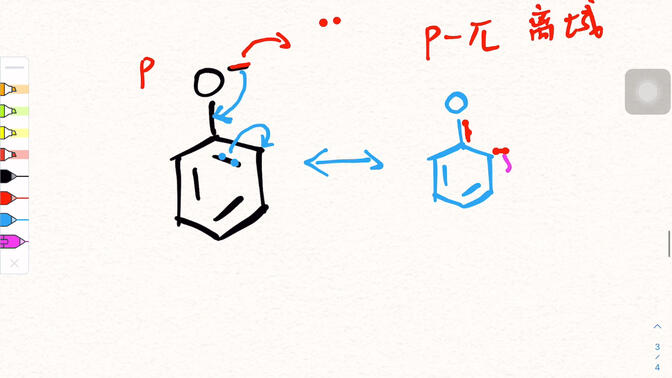
Struktur resonans phenol boleh dibentangkan melalui gambarajah skematik mudah.
Struktur asas phenol adalah kumpulan hidroksil (- OH) yang melekat pada cincin benzena.
Persamaan had resonans adalah struktur asal phenol, di mana atom oksigen lone pasangan elektron tidak terlibat dalam delocalization;
Dalam persamaan had lain, elektron pasangan lone atom oksigen berinteraksi dengan besar & pi; - bon cincin benzene, membentuk suatu bon double separa ciri-ciri antara atom oksigen dan cincin benzene. Pada masa yang sama, ketumpatan awan elektron bersebelahan dan perenggan pada cincin benzena meningkat, dan arah pergerakan elektron ditunjukkan oleh anak panah. Persamaan had berbilang superimposed untuk menggambarkan pengagihan awan elektron benar phenol.
3. Manifestasi struktur resonans dalam tindak balas phenol
1. Kes-kes tertentu tindak balas
Reaksi phenol dengan air bromine adalah kes klasik. Apabila air bromine ditambah dropwise kepada penyelesaian phenol, mendak putih yang dihasilkan dengan serta-merta, yang tribromophenol.
2. Digabungkan dengan analisis struktur resonans
Dari sudut pandangan struktur resonans, atom bromine adalah lebih cenderung untuk menyerang dua jawatan ini disebabkan oleh ketumpatan tinggi ortho-dan perenggan-elektron awan phenol. Semasa tindak balas, atom bromine secara beransur-ansur menggantikan atom hidrogen pada cincin benzena, dan akhirnya mendakan putih tribromophenol dihasilkan. Proses ini jelas menunjukkan peranan penting struktur resonans dalam menjelaskan tindak balas kimia fenol.
3. Menekankan peranan struktur resonant
Melalui kes ini, kita mempunyai pemahaman yang lebih mendalam tentang struktur resonans bukan sahaja konsep teori, tetapi juga kunci untuk memahami sifat tindak balas kimia fenol. Ia adalah seperti satu pengalir senyap, membimbing tindak balas kimia.
4. Nilai dan prospek mengkaji struktur resonans phenol
Struktur resonans menjadikan phenol mempunyai kereaktifan yang unik, keasidan dan kestabilan, yang seterusnya menentukan penggunaan phenol dalam pelbagai bidang. Pada masa akan datang, kita boleh menggabungkan kaedah kimia pengkomputeran maju dan teknik eksperimen untuk mengkaji struktur resonans fenol. Ini akan membantu kita memahami sifat dan tingkah laku fenol lebih komprehensif, memberikan sokongan lebih teori dan bimbingan praktikal untuk pembangunan kimia organik, dan biarkan "generalist dalam" phenol memainkan peranan yang lebih besar dalam lebih banyak bidang.

